
| 分子诊断技术
分子诊断是应用分子生物学的方法检测患者体内遗传物质的结构或表达水平的变化而做出诊断的技术。临床上目前应用较多的分子诊断技术主要包括荧光原位杂交(FISH)、聚合酶链式反应(PCR)、基因芯片和基因测序(NGS高通量测序)。
核心分子诊断技术发展图示
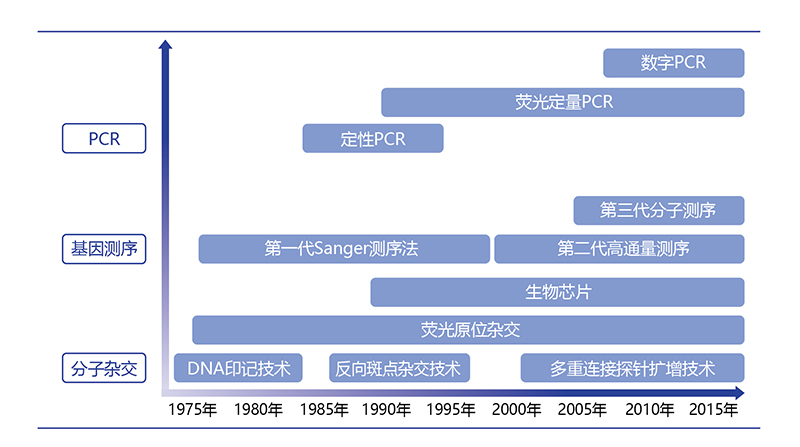
其临床上的应用非常广泛,从最初的病原微生物的核酸诊断、遗传疾病的特征序列诊断,到如今个体化用药伴随基因诊断、NIPT和肿瘤的测序诊断,已逐渐扩展至全疾病谱。其中肿瘤基因检测将有助于实现从化疗到个体化治疗的精准治疗升级:小分子靶向药、大分子单抗药、免疫检查点治疗、CAR-T治疗等均需要筛选病人的遗传特征才能发挥最大疗效。

| 分子诊断标准品和参考品
分子诊断(基因检测)涉及的环节较多,从不同的样品制备到仪器校准,几乎工作流程的每一步都可能产生不准确的结果,这使得分析结果存在假阳性或假阴性的可能。
要提高基因检测准确度,控制检测过程中的变量,需要从以下两个重要环节着手:
1. 实验室检测性能的验证
使用标准品对实验室的仪器设备耗材人员环境等进行验证(EQA测评)。
2. 质控品的覆盖范围和使用率
提高质控品的覆盖范围和使用率
| NGS流程—分子诊断检测流程长,缺乏规范,每个步骤极易引入变量

在这两个环节的控制上标准品的作用不可替代:
标准品的需求贯穿基因检测实验全流程:样品处理-DNA提取-DNA定量-建库效率-产出监控-数据校准-分析和诊断。
质控品评价整个检测流程的有效性和可信度。
| 分子诊断标准品研制的技术要求
原材料应尽可能与临床样本相一致或接近,主要来源于临床样本、永生化细胞系、基因编辑细胞系,也可来自基因工程构建产品及重组质粒。需采用国内外公认的方法进行验证,具备均匀性和稳定性,批间变异性应小于分析系统的变异,在规定的条件下有良好的稳定性。可单批大量获得。
| 分子诊断标准品的生产方式
1. 临床收样建系
遗传性疾病大多数都是通过胚系基因遗传引起的,可以通过收集临床样本,并对这些样本的衍生物进行细胞系永生化研发和生产标准品,以满足试剂盒开发公司及临床检测的要求。
2. 基因编辑
对于病人资源不易获得的位点,作为前一种方法的补充,也采取细胞编辑的方法进行标准品生产。
由于临床样本珍贵,不可再生,不可长期稳定的提供,且突变情况未知,突变频率不清楚,且有伦理法规限制,较难商业化应用。然而室内质控和日常质控是长期的规范操作,需要可持续的常规化制备质控品。
因而目前普遍接收细胞系来源标准品: 可以模拟临床样本,明确的突变位点,明确的突变频率,能够反应实际的临床样本检测所有出现的现象。

而基因编辑方法则可以制备的成对细胞系,可提供阶梯性标准品:
1. 等位基因母细胞
2. 等位基因人工变异后细胞
将二者混合制备不同突变比例的标准品,可以提供实验室检测极限性能验证的标准品
| 分子诊断标准品在IVD(体外诊断)产业链中的应用
· IVD产业链上游:
NGS/qPCR/ddPCR仪器研发生产,酶引物等原料研发生产
帮助性能验证和注册保证
· IVD产业链中游:
IVD试剂盒研发
优化验证新Pannel
流程优化/性能检测
企业参考盘注册申报
生产质检
· IVD产业链下游:
药企伴随诊断,LDT检测,医检所检测,医院病理科/检验科检测
日常质控,平台对比,EQA支持,检测限检测
患者治疗用药
| 海星生物HyCyteTM基因检测标准品特点
· 可再生
· 有类似检测样本的基因组复杂结构(异质性)
· 有明确的拷贝数和等位基因数
· 质量高度稳定、均一性好
· 具有临床标本和肿瘤细胞的特性
· 无伦理风险
海星生物专注细胞基因编辑(基因敲除\敲入\突变\过表达)十年:为基因检测提供参考品细胞株开发,已经和多家基因诊断公司建立合作。海星生物可以提供诊断试剂盒标准品定制化服务,为客户定制拷贝数固定(或高突变频率)的单核苷酸变异(SNV)、碱基缺失(Deletion)、碱基插入(Insertion)、基因融合(Fusion)、拷贝数变异(CNV)等各种变异类型的标准品细胞株,可应用于基因检测的上游试剂盒研发、企业参考盘注册申报、生产质检,下游ICL的日常质控、EQA支持。解决临床样本有限,稀有突变难获得的问题。还可以订制开发IHC(免疫组化)标准品细胞株,解决细胞系表达丰度不稳定,染色深浅不一的问题。此外针对肿瘤早筛甲基化检测试剂盒,海星生物可以提供低甲基化水平DNA参考物质。
 客户成果
客户成果
 客户成果
客户成果

 案例分析
案例分析
 案例分析
案例分析
 参考文献
参考文献
 参考文献
参考文献